Programme de recherche : Axes
Accueil > Équipe 3 > Programme de recherche > Axe 3
Pollution de l’air et emphysème pulmonaire : impacts sur la fonction musculaire squelettique
Pascal Pomiès, Emilie Passerieux, Anne Virsolvy, Fares Gouzi, Maurice Hayot
Une conséquence extra-pulmonaire importante de la bronchopneumopathie chronique obstructive (BPCO) est la dysfonction musculaire périphérique qui se traduit chez les patients par une intolérance à l’effort, une qualité de vie amoindrie et un taux de survie plus faible. Cette dysfonction musculaire se caractérise par une faiblesse et une atrophie musculaires. Une des hypothèses actuelles est que la dysfonction musculaire provient d’un micro-environnement délétère dû à une inflammation systémique importante chez le patient BPCO stable voire amplifiée chez le patient BPCO en exacerbation. Nous développons actuellement des études translationnelles afin d’évaluer les mécanismes impliqués dans cette dysfonction musculaire et de tester différentes approches thérapeutiques.
Objectif 1 : Un modèle cellulaire pour l’étude de la dysfonction musculaire in vitro.
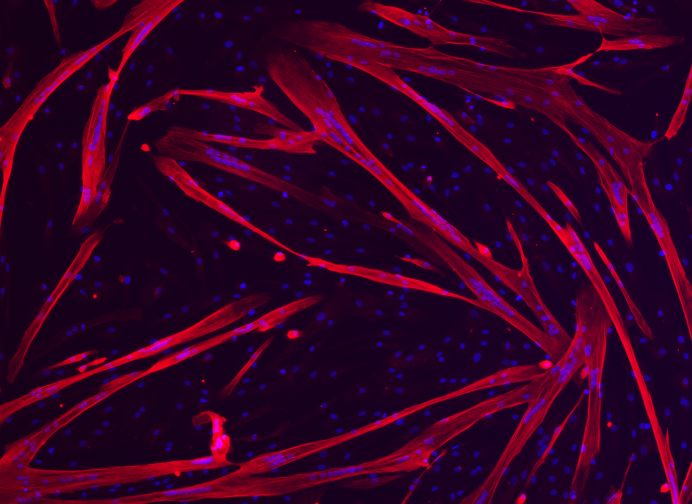
Myotubes BPCO en culture
Nous avons développé et validé un modèle cellulaire in vitro de l’altération musculaire dans la BPCO à partir de cellules satellites issues de patients. Nous avons montré que les myotubes BPCO présentaient une atrophie associée à un stress oxydant élevé comparable à ce qui est observé dans le muscle BPCO in vivo (Pomiès et al. 2015 ; 2016 ; Gouzi et al. 2018).
Nous étudions actuellement des défauts potentiels de la fonction musculaire (régénération, différenciation, contraction) à l’aide de ce modèle cellulaire soumis à diverses stimulationsin vivo (Catteau et al. 2021).
Objectif 2 : Impact du micro-environnement inflammatoire sur la dysfonction musculaire chez le patient BPCO.
Nous évaluerons le niveau d’expression d’un panel de molécules pro-inflammatoires dans le sérum de patients BPCO de différents stades (léger, sévère, en exacerbation) afin de déterminer des biomarqueurs cibles. L’effet délétère sur le muscle de ces différents microenvironnements en fonction du profil inflammatoire des patients sera alors testé sur notre modèle cellulaire par l’étude de différentes voies de signalisation (régénération, différenciation, atrophie) dans le but de cibler un candidat thérapeutique potentiel(Catteau et al. 2020).
Objectif 3 : Un modèle animal de la BPCO : le rat élastase-LPS
Nous utilisons actuellement un modèle de rat élastase-LPS, commun à l’équipe, qui mime les altérations pulmonaires et extra-pulmonaires de la BPCO. Nous évaluons actuellement les effets du traitement élastase-LPS sur l’altération musculaire (contractilité in vivo, in vitro, atrophie). Ce modèle animal nous permettra d’évaluer les effets thérapeutiques de diverses molécules et interventions non-médicamenteuses sur le muscle squelettique.
Mots clés : BPCO, muscle squelettique, atrophie, micro-environnement, modèle cellulaire, cellule satellite, inflammation, biomarqueurs, modèle animal

